IGF –Insulin Growth Factors (English text below)
Les « insuline-like growth factors (IGF) » ont été découverts en 1956 par William D. Saumon Jr. et William H. Daughaday à la Washington University, St Louis, Etats-Unis (1).
Au départ, les IGF sont appelés facteurs de sulfatation parce qu'ils étaient en mesure de remplacer l''activité du facteur de sulfatation de l'hormone de croissance (GH).
En outre, l’activité des IGF a été démontrée dans la stimulation de la synthèse d'ADN (2), la synthèse de protéoglycanes (3), la synthèse des glycosaminoglycanes (4), et la synthèse des protéines (5).
En 1963, al Froesch et al. de l'Université de Zorich, Suisse, décrit l’activité insuline dans le sérum (6). Seule une petite fraction de l'activité insulinique du sérum normal sur le tissu adipeux et le muscle pourrait être bloquée par les anticorps spécifiques contre l'insuline. Le médiateur de cette activité insulinique n'était pas détectable avec le dosage radio-immunologique développé pour l'insuline en 1959, et a été nommée activité non-suppressible de type insuline (NSILA) (6).
Dulak et Temin ont démontré une activité mitogène en milieu sérum-free de lignées cellulaire d'hépatome de rat, qu’ils ont appelé multiplicationstimulating activity (MSA) (7).
En 1972, ces trois peptides apparemment distincts (facteur de sulfatation, NSILA, MSA) ont été unifié sous le terme somatomédine, car il semble influencer les actions de la GH (également appelée somatotropine) (8).
En 1978 Rinderknecht et Humbel ont purifié à partir de sérum la somatomédine, et il s'est
avéré qu’elle était constituée de deux peptides étroitement liés, qui ont été appelés Insulin-like growth facteur-I (IGF-I) et d’Insuline-like growth factor-II (IGF-II) (9, 10).
Aspects évolutifs
La molécule d'IGF-I est conservée tout au long de l'évolution des vertébrés (11).
Amphioxus, un protochordé (ancêtre des vertébrés), exprime une molécule hybride insuline / IGF-I (12). Ceci suggère fortement que les IGF-I ont divergé de la ligne principale de l'évolution de l'insuline à un stade précoce de l’évolution des vertébrés.
Stucture et expression du gène de l'IGF-I
Chez l'homme le gène de l'IGF-I est une isolé sur le chromosome 12 et constitué d'au moins six exons (13). Bien que le foie soit considéré comme le seul producteur de l'IGF-I, des études récentes ont montré que la plupart des tissus expriment l'IGF-I (14). L'expression de l'ARNm de l'IGF-I résultant de différentes sites d'initiation de la transcription est tissu-spécifique et régulé par le système hormonal (11).
Stucture de l'IGF-I
L‘ IGF-I, l’IGF-II et l'insuline sont les membres d'une famille de polypeptides qui sont caractérisés par un degré élevé d'homologie de séquence (15) (voir figure 1). L’IGF-I a
50 à 60% d'analogie avec l'insuline humaine (16). L’IGF-I est d’abord synthétisée sous forme d'un pré-IGF contenant un peptide de base, ainsi que d'un peptide d'extension, le peptide E (17).
Le peptide de base et le peptide E sont ensuite clivés lors du traitement de l'IGF-I mature (17). L’IGF-I est un peptide de 70 acides aminés, qui est différente de l’insuline ; l'extrémité carboxy- contient une séquence du domaine D supplémentaire (18).
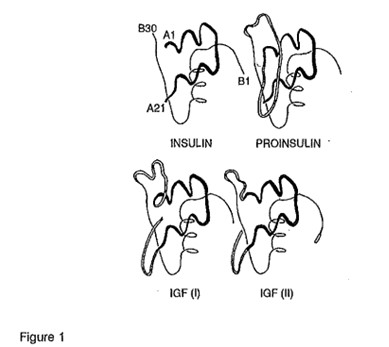 Figure 1
Figure 1
Structure de la famille peptidique de l'insuline-like growth factor. Le trait épais représente la chaîne A, les doubles lignes représentent le prolongement D et la chaîne C reliant les chaînes A et B (de Le Roith D. Insulinlike growth factors in health and disease. Ann Intern Med 1992; 116: 855; with permission from the American College of Physicians)
L’IGF-I purifié à partir de cellules du cerveau, du colostrum bovin et de l'utérus présente un déficit de trois acides-aminés (Gly-Pro · glu) (19). Cette forme tronquée de l'IGF-I, appelée des-IGF-I, a une activité biologique plus grande que l’IGF-I parce qu'elle a une plus faible affinité pour la protéine de liaison insuline-like growth factor protéin (IGFBP) (voir ci-dessous). Il est donc plus disponible pour interagir directement avec le récepteur de l'IGF-I. Le clivage du tripeptide se produit probablement après la synthèse, bien que les biomécanismes responsables n'aient pas encore été identifié.
Fonctions de l'IGF-I
L’IGF-I exerce de nombreuses fonctions biologiques sur les tissus cibles lointaines via la circulation sanguine (effets endocriniens), sur ses propres cellules d'origine (effets autocrines), et sur les tissus voisins (effets paracrines) (20). L’IGF-I est à la fois anabolisant et mitogénique, que ce soit in vitro et in vivo, et ses effets se recoupent souvent avec les effets biologiques de l'insuline. (Voir Tableau 1 ci-dessous).
(20 à 23): l’IGF-I stimule la différenciation des cellules et est un agent mitogène des cultures cellulaires via la stimulation de l’incorporation de thymidine dans l'ADN et d’uridine dans l'ARN (21).
In vitro la glycogenèse, l'absorption des acides aminés et les échanges d’ions sont augmentées par l'IGF-I (21).
In vivo, l'IGF-I stimule la croissance en longueur des os et diminue la sécrétion de GH et d'insuline (20).
Chez des volontaires humains sains perfusés avec des solutions d’IGF, on constate une meilleure 'absorption du glucose, une diminution des acides gras libres des taux de triglycérides, et une diminution de la dégradation des protéines (20).
De plus, l'insuline stimule la synthèse hépatique des IGF-I (24). L’IGF-I, à son tour, inhibe la sécrétion de l'insuline même dans des conditions euglycémiques (25).
Administrés à des patients soumis à des rations hypocaloriques les IGF-I améliorent le bilan azoté (26). Les IGF-I augmentent le taux de filtration glomérulaire et le flux plasmatique rénal et améliorent aussi la clairance de la créatinine (27).
L’IGF-I influence donc de nombreuses fonctions cellulaires et est considérée comme un facteur de croissance et une hormone anabolisante, ayant aussi d'importantes fonctions de régulation métabolique.
Une autre action des IGF-I, complémentaire des effets sur la prolifération cellulaire, est la capacité à inhiber la mort cellulaire programmée dans certaines cellules, appelée aussi l'apoptose (28, 29).

La concentration en Insulin-like growth factor-I libre
L’IGF-I libre, par analogie avec les stéroïdes sexuels et les glandes surrénales et les hormones thyroïdiennes, est la forme active biologique majeure hormonale de l'IGF-I (30) (figure 2). La détermination de la fraction sérique libre d'IGF-I (non liée) n'a pas été possible jusqu'à très récemment (30, 31).
En 1994, Frystyk et al. et Lee et al décrivent séparément une méthode pour déterminer la fraction libre d’IGF-I dans le sérum (30, 31).
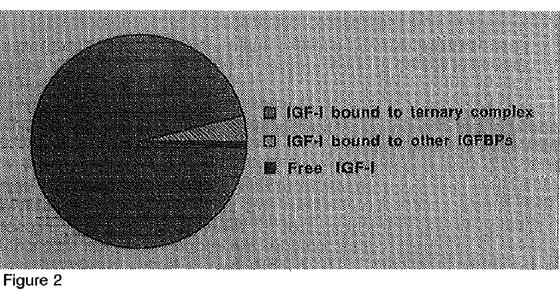
Figure 2 : Répartition des IGF dans le sérum. Quatre-vingt quinze pour cent des IGFs se trouvent dans le cadre du complexe ternaire de l'IGF-I et IGF-II lié à l'IGFBP-3 et à une sous-unité (ALS). Moins de 5% sont liés à d'autres IGFBP, et une très petite composante circule comme forme libre (Collett-PF Solberg, Cohen P.)
La plupart des IGF-I circulants est lié aux protéines d'insuline-like growth factor (IGFBP), qui indique la disponibilité de l'IGF-I à ses récepteurs dans les tissus cibles, tandis qu'une très petite partie circule comme forme libre (32). Les niveaux des IGF-I libre dans un tissu sont modulés par le taux de production d'IGF-I, et le degré de liaison à l’IGFBP (33). La clairance métabolique sérique d’IGF-I est estimée à 2,62 ± 0,94 ml / min avec un taux de production de 4,75 ± 1,74 mg / jour (621 ± 227,34 nmol / jour) (34).
La biodisponibilité de l’IGF-I est probablement un facteur important dans la détermination des différentes fonctions physiologiques de l’'IGF-I et l'insuline (20).
Le récepteur de l'IGF-I
Il existe au moins deux catégories de récepteurs à l’IGF-I: le récepteur IGF-I et le récepteur IGF 11 / mannose-6-phosphate (Man-6-P) (35).
Le récepteur de l'IGF-I, comme le gène du récepteur de l'insuline, se compose de 22 exons (36). Il est le produit d'un gène copiant unique situé à l’extrémité distale du chromosome 15 (37).
Les récepteurs d’IGF-I sont exprimé dans de nombreuses cellules, dans de nombreux tissus (38).
Le chevauchement biologique des effets des IGF et de l'insuline ont été initialement attribués à des analogies de structure entre les peptides eux-mêmes, mais cette interprétation s'est avéré être trop simple, après qu'il a été montré que les récepteurs de l'insuline et de l'IGF-I sont également structurellement similaire (39) (figure 3).
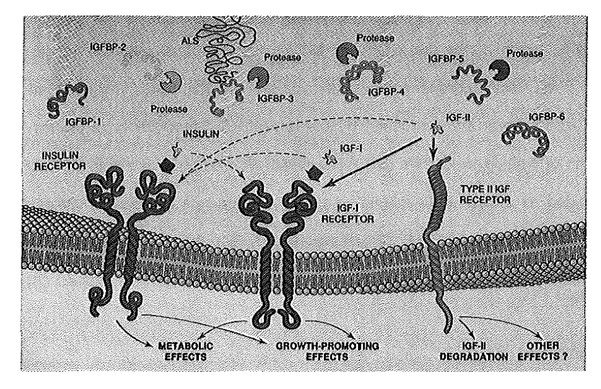
Figure 3 La famille de peptides IGF circulants (à partir : Lowe WL insuline-like growth Factors. Science & Medicine, 1996, 3: 65; avec la permission de Science & Médecine)
En outre, l'IGF-I, IGF-II et l'insuline peuvent se lier avec les mêmes récepteurs. (15).
Le récepteur de l'IGF-I se lie préférentiellement l'IGF-I, mais se lie également avec l’IGF-II et plus faiblement avec l’insuline.
Le récepteur de l'IGF-II se lie IGF-II avec une plus grande affinité que l'IGF-I, mais n'interagit pas avec des concentrations plus élevées de l'insuline (40).
Parce que l'IGF-I, IGF-II et l'insuline peuvent produire les mêmes réponses biologiques, et parce que de nombreuses cellules possèdent des récepteurs IGF-I, IGF-II ainsi que des récepteurs de l'insuline, il a été difficile de déterminer quel récepteur est la médiation d'une réponse particulière (40).
Les tentatives visant à évaluer les contributions relatives de ces trois récepteurs à une la réponse biologique ont tenu compte :
1] de la détermination des récepteurs présents sur un type cellulaire et les affinités de liaison pour ces trois ligands,
2] de la détermination de la relation dose-réponse biologique à l'IGF-I, IGF-II et l'insuline et 3] du blocage sélectif de l'IGF-I ou récepteurs de l'insuline avec des anticorps anti-récepteur spécifiques intrinsèques sans effets biologiques (40).
Ces recherches ont montré que l'insuline et les hormones IGF sont complémentaires dans leur action anabolisante : l'insuline et les récepteurs de l'insuline sont particulièrement impliqués dans la régulation des fluctuations à court terme des principaux métabolites tels que le glucose, les acides aminés et les acides gras libres. Les IGF et le récepteur de l'IGF-I sont particulièrement impliqués dans la régulation des processus de longue durée qui sont responsables de la croissance cellulaire et la différenciation (41).
Dans certains tissus et de cellules exprimant à la fois un nombre élevé de IGF-I et de récepteurs à 'insuline, des récepteurs hybrides peuvent se former (11). Ces hybrides sont des récepteurs tétramères composés d'un hétérodimère du récepteur de l'insuline liée par des ponts disulfure à un hétérodimère de récepteur de l'IGF-I. Un rôle possible pour ces récepteurs hybrides est que ils pourraient servir de médiateurs à des fonctions communes, où, sous certaines circonstances, l’insuline doit induire la prolifération cellulaire et de l'IGF-I peut stimuler les fonctions métaboliques (11).
On suppose que la plupart des effets biologiques de l'IGF-II sont médiés par le récepteur IGF-I (42).
Les protéines de liaison des IGF (IGF Binding Protein IGFBP).
Les IGFBP sont une famille de protéines qui se lient de façon non covalente avec les IGF-I et IGF-II avec une haute affinité (constante de dissociation de l'ordre de grandeur de 10-11 molL) et spécificité (tableau 2) (43, 44).

À ce jour, au moins six IGFBP ont été identifiés (20,33). Elles ont un haut degré d'analogie de séquence (44) et sont numérotées de 1 à 6 dans l'ordre dans lequel leur structure primaire a été déterminée (45) (figure 3).
Les semblent avoir quatre grandes fonctions qui sont essentielles pour coordonner et réguler les activités biologiques de l'IGF-I:
l- d'agir comme le transport protéines de transport dans le plasma et de contrôler le flux sortant de l'IGF-I et IGF-II à partir de l’espace vasculaire ;
2- de prolonger la demi-vie de l'IGF-I et IGF-II et ainsi réguler la clairance métabolique ;
3- de fournir un signal tissu-et cellules-spécifique ;
4- de moduler directement l'interaction entre l'IGF-I et le récepteur IGF-I et , par conséquent, indirectement commander son action biologique (20).
L’IGFBP va non seulement réguler la biodisponibilité de l'IGF-I, mais semble également avoir leurs propres récepteurs, qui assurent la médiation l’action de l'IGF-I libre (33).
Les IGFBP sont produits par une grande variété des tissus différents, dont chacun contient des niveaux spécifiques de ces IGFBP (33).
Le clivage des IGFBP par l'IGFBP-protéase joue un rôle clé dans la régulation de la fraction libre des IGF et agit par deux mécanismes :
1- La liaison de l’IGFBP à l’IGF va diminuer la concentration de l'IGF-I libre disponible pour interagir avec le récepteur de l'IGF-I, et
2- Le clivage des IGFBP en fragments avec une plus faible affinité pour l'IGF-I permet d’augmenter l'activation du récepteur (33).
Dans divers systèmes biologiques il a été observé que les IGFBP peuvent empêcher ou potentialiser l'action des IGF-I (41).
L’IGFBP-l et d'IGFBP-3 sont étudiés plus en détail, parce que le rôle des quatre d'autres protéines de liaison est moins bien établie à l'heure actuelle.
L’IGFBP-l est une KD 25 protéine et est trouvée en concentrations élevées dans le liquide amniotique (32). L’IGFBP-l est sécrétée par les hépatocytes, les reins, la decidua et l'endomètre (33). La demi-vie d'élimination plasmatique est environ 90 minutes (46). L’IGFBP-l a été proposée comme un régulateur clé de l'activité d'IGF-I (47). L'insuline est un régulateur majeur de la production hépatique de l'IGFBP-l (33): les taux plasmatique d’IGFBP-l sont inversement liés aux niveaux d'insuline in vivo (48).
L’IGFBP-l existe sous différentes formes (phosphorylée et non phosphorylée) (49). La fraction non phosphorylée IGFBP-l a une plus faible affinité (4 - à 6-fois) pour l'IGF-I que la fraction phosphorylée (49). Cela favoriserait la séquestration de l'IGF-I par la fraction phosphorylée et une affinité plus complète de l'IGF-I à son récepteur avec la forme non-phosphorylée. La plupart des études ont montré une inhibition de l’IGF-I par la forme phosphorylée (20). La forme IGFBP-l qui potentialise l'activité IGF-I est non phosphorylée, a une plus faible affinité et est capable de s'associer à la surface de la cellule (50).
L’IGFBP-l stimule aussi la migration cellulaire (51). Le stimulus apparaît pour la fixation de l'IGFBP-l à une intégrine sur la surface cellulaire, via l'ouverture d'une voie intracellulaire qui implique une série de kinases (45).
Quantitativement, la fraction la plus importante d’IGFBP dans la circulation est l’IGFBP-3 (52). Les complexes 150 kD consistent en IGF-I (ou IGF-II), l'IGFBP-3, et une sous-unité labile en milieu acide (ALS), qui est glycosylé et ne se lie pas l'IGF-I (53). L'ALS est présent en excès dans du plasma humain et l'hormone de croissance est dépendante (53, 54). L’IGFBP-3 est sécrétée par hépatocytes et de nombreuses autres cellules. Environ 75-95% de l'IGF-I dans la circulation est liée à ce complexe IGF-I IGFBP3 (20, 33) (voir figure 2). Il est considéré comme un réservoir pour l'IGF-I dans la circulation : Le complexe 150 kD ne peut pas traverser la barrière endothéliale des vaisseaux sanguins (52). Ceci est considéré comme essentiel pour éviter un effet d'hypoglycémie du aux fortes concentrations d'IGF-I, qui sont présents dans le plasma (52).
La liaison de l'IGF-I dans le complexe de 150 kD allonge sa demi-vie dans le plasma de 10 minutes sous sa forme libre à 12 à 15 heures, s'il est lié à la forme complexe (55).
L'expression du gène codant pour l'IGFBP-3 est augmentée par p53, un gène suppresseur de tumeur, qui est considéré comme important dans l'inhibition de formation de tumeur (56). Récemment, il a été démontré que l'IGFBP-3 produit en réponse à p53 est capable d'inhiber l'IGF-I qui induit la croissance des cellules (56). L’IGFBP-3 apparaît ainsi comme l'une des protéines qui assurent la médiation des effets de p53 sur la croissance cellulaire, éventuellement par l'apoptose.
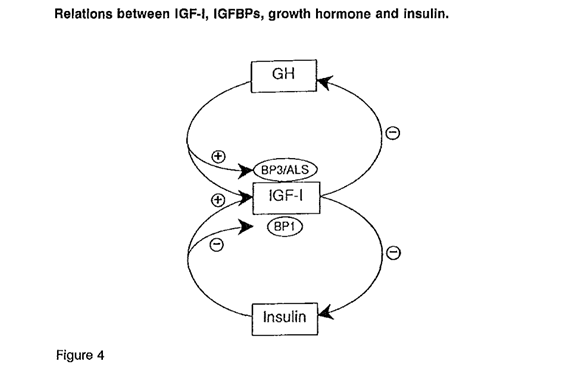
Figure 4 Les relations entre l'IGF · I, l’IGFBP, l'hormone de croissance et l'insuline {from : Bondy CA. Facteur de croissance des utilisations cliniques de l'insuline-like. Ann Intern Med 1994 ; 120 : 594 ; avec la permission de l'American College of Physicians)
L'hormone de croissance (GH) et l’insuline stimulent la sécrétion hépatique d'IGF-I, et l’IGF-I exerce un feed-back négatif pour diminuer la sécrétion de GH et de l'insuline.
L’IGFBP-3 et la sous-unité labile en milieu acide (ALS) sont positivement régulée par la GH, tandis que les taux de IGFBP-1 sont régulé négativement par l'insuline (40) (figure 4).
IGF-I et l'âge
L'âge est un déterminant majeur des concentrations plasmatiques d'IGF-I (57). Les taux sériques de IGF-I augmentent de manière significative par rapport aux niveaux très faibles dans le sérum du cordon à partir des premier 9 mois de la vie, après quoi il ya une augmentation quasi linéaire.
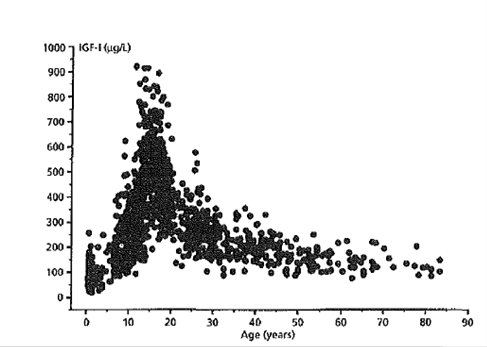
Figure 5
Taux sériques d'IGF-I (axe vertical) en fonction de l'âge (axe horizontal) tout au long de
la vie dans une population humaine en bonne santé (n = 1236 sujets). Notez le pic à la puberté et le large éventail de niveaux de IGF I · (Ph D Thesis, Université de Copenhague, 1995 ; avec la permission de Novo Nordisk, Danemark)
Après la puberté, on observe une diminution (de 250%) des valeurs sériques d’IGF1. On considère que cette diminution est due en partie à la diminution de sécrétion de la GH. On en sait encore peu sur les effets et les conséquences cliniques de la diminution de la GH.
IGF-I et le diabète
Beaucoup de patients avec diabète insulino-dépendant de type 1 ont un certain degré de résistance à l'hormone de croissance, comme le montre la diminution des taux d’IGF-I, en dépit de l’augmentation des concentrations de GH (59-61). Ces niveaux élevés n'ont pas la capacité de produire une augmentation appropriée du taux d'IGF-I en réponse à GH exogène. Cette baisse d’affinité à la GH peut être due à la diminution de l’insuline dans le réseau veineux hépatique (40). Le traitement par injections d'insuline sous-cutanée ne peut pas normaliser toutes les fonctions du foie, comme la synthèse d'IGF-I, qui dépend principalement de la présence des taux élevés d'insuline veineux (40). En outre, l'augmentation des niveaux d'hormone de croissance peut aggraver l'hyperglycémie et de faibles niveaux d'IGF-I peuvent également contribuer à la déficience du métabolisme du glucose et de l'hyperglycémie (40).
L'hyperglycémie est considéré comme un facteur pathogénique important pour le Développement de complications diabétiques micro-et macro-vasculaires (62).
References
- Salmon WO, Oaughaday WHo A hormonally controlled serum factor which stimulates sulfate incorporation by cartilage in vitro. J Lab Clin Med 1957; 49: 825-836.
- Oaughaday WH, Reeder C. Synchronous activation of DNA synthesis In hypophysectomized rat cartilage by growth hormone. J Lab Clin Med 1966; 68: 357-368.
- Hall K, Uthne K. Some biological properties of purified sulfation factor (SF) from human plasma.
Acta Med Scand 1971; 190: 137-143.
- Oaughaday WH, Philips LS, Herington AC. Measurement of somatomedln by cartilage in vitro.
Methods Enzymol 1975; 37B: 93·109.
- Salmon jr WO, Duvall MR. In vitro stimulation of leucine incorporation into muscle and cartilage protein by a serum fraction with sulfation factor activity: differentiation of effects from those of growth factor and Insulin. Endocrinology 1970; 87: 1168-1180.
- Froesch ER, BOrgi H, Ramseier EP, Bally P, labhart A. Antibody suppressible and insulin-like activities In human serum and their physiological significance. An insulin assay with adipose tissue of increased precision and specificity. J Clin Invest 1963; 42: 1816-1834.
- Dulak NC, Temin HM. A partially purified polypeptide fraction from rat liver cell conditioned medium with multiplication·stimulating activity for embryo fibroblasts. J Cell Physiol1973; 81: 153- 160.
- Daughaday WH, Hall K, Raben MS, Salmon WD, van den Brande JL, van Wyk JJ. Somatomedin: proposed designation for sulfation factor. Nature 1972; 235: 107-108.
- Rinderknecht E, Humbel RE. The amino acid sequence of human Insulin-like growth factor I and its structural homology with proinsulin. J Bioi Chem 1978; 253: 2769-2776.
- Rinderknecht E, Humbel RE. The primary structure of hUman insulin-like growth factor II. FEBS Letters 1978; 89: 283-286.
- LeRoith D, Adamo M, Werner H, Roberts CT. Molecular and cellular biology of the Insulin·like growth factors, in: Weintraub BO (editor), Molecular Endocrinology, basic concepts and clinical correlations, Raven Press, New York, USA, 1995, pp 181-193. 12. Chan SJ, Cao Q-P, Steiner OF. Evolution of the insulin superfamily: cloning of a hybrid Insulin/lnsulin-like growth factor cDNA from amphioxus. Proc Natl Acad Sci USA 1990; 87: 9319-
9323.
- Brissenden JE, Ulrich A, Francke U. Human chromosomal mappIng of genes for insulin-like growth factors I and 11 and epidermal growth factor. Nature 1984; 310: 781-784.
- LeRoith O. Insulin-like growth factors in health and disease. Ann Intern Med 1992; 116: 854- 862.
- Froesch 'ER, Zapf J. Insulin-like growth factors and insulin: comparative aspects. Diabetologla 1985; 28: 485·493.
- Van den Brande Jl. Structure of the human Insulin-like growth factors: relationship to function. In: Schofield PN (editor), The insulin-like growth factors, structure and biological functions, Oxford University Press, Oxford, UK, 1992, pp 12-44.
- Daughaday WH, Rotwein P. Insulin-like growth factors I and II. Peptide, messenger ribonucleic acid and gene structures, serum, and tissue concentrations. Endocr Rev 1989; 10: 68-91.
- Sara VR, Hall K. Insulin·like growth factors and their binding proteins. Physiol Rev 1990; 70: 591-594.
- Sara VR, Carlsson-Skwirut C, Andersson C, Hall E, Sjogreb B, Holmgren H, Jornvall H. Characterization of somatomedlns from human fetal brain; Identification of a variant form of insulinlike growth factor I. Proc Nail Acad Sci USA; 1986; 83; 4904-4907.
- Jones JI, Clemmons DR. Insulin-like growth factors and their binding proteins: biological actions. Endocr Rev 1995; 16:3-34. 21. Kless W, Kessler U, Schmitt S, Funk B. Growth hormone and Insulin-like growth factor-I: Basic aspects. In: Flyvbjerg A, 0rskov H, Alberti KGGM (editors), Growth hormone and inSUlin-like growth factor-' in human and experimental diabetes, John Wiley & Sons, Chlcester, UK, 1993, pp 1-21.
- Froesch ERr Schmid C, Schwander J, Zapf J. Actions of insulin-like growth factors. Ann Rev Physiol1985; 47: 443·467.
- Kahn CR. The molecular mechanism of Insulin action. Ann Rev Med 1965; 36: 429·451.
- Phillips LS, Harp JBr Goldstein S, Klein J, Pao CI. Regulation and action of Insulin·like growth factors at the cellular level. Proc Nutr Soc 1990; 49: 451-456.
- Rennert NJ, Caprio S, Sherwin RS. Insulin·like growth factor-I inhibits glucose-stimulated insulin secretion but does not impair glucose metabolism in normal humans. J Clin Endocrinol Metab 1993; 76: 804·806.
- Clemmons DR, Smith· Banks A, Underwood LE. Reversal of diet-induced catabolism by infusion of recombinant insulin·like growth factor-I (IGF-I) in humans. J Clin Endocrinol Metab 1992; 75: 234- 238.
- Hirschberg R Brunori G, Kopple JD, Guier HP. Effects of insulin-like growth factor I on renalfuncUon In normal men. Kidney Int 1993; 43: 367-397,
- Muta K, Krantz SB. Apoptosis of human erythroid colony forming cells is decreased by stem cell factor and insulin· like growth factor-I as well as erythropoietin. J Cell Physlol 1993; 156: 264-271.
- Kaleko M, Rutter WJ, Miller AD. Overexpresslon of the insulinlike growth factor receptor promotes ligand-dependent neoplastic transformation. Mol Cell Bioi 1990; 10: 464·473.
- Frystyk J, Skjrerbrek C, Dlnesen B, 0rskov H. Free Insulin·like grow1h factors (IGF-I and IGF·II) in human serum. FEBS letter 1994; 348,185-191. 31. Lee PDK, Powell 0, Baker B, Liu F, Mathew G, Levitsky I, Gutierrez 00, Hintz RL.
Characterization of a direct, non·extractlon Immunoradiometric assay for free IGF-1. Abstract 939, Presented at the 76th annual meeting of the Endocrine Society, Anaheim 1994.
- Drop SL, Kortleve OJ, Guyda HJ. Isolation of a somatomedin·blnding protein from preterm amniotic fluid. Development of a radioimmunoassay. J Clin Endocrinol Metab 1984; 59: 899-907.
- Collett-Solberg PF, Cohen P. The role of insulin·like growth factor binding proteins and the IGFBP proteases in modulation of IGF action. Endocrinol Metab CUn North Am 1996; 25: 591-614.
- Boroujerdl MAt Jones RH, Sonksen PH, Russell·Jones DL. Stimulation of IGF·I pharmacokinetics after infusion of recombinant IGF-Iln human subjects. Am J Physiol 1997; 273: E438·E447.
- Baxter RC. Insulin-like growth factor binding proteins in human circulation, a review. Horm Res 1994; 42: 140-144.
- Undenwood LE, van Wyk JJ. Normal and aberrant grow1h. In: Wilson JD, Foster OW (editors), Williams Textbook of Endocrinology, WB Saunders Company, Philadelphia, USA, 1992, pp 1079· 1138.
- Ullrich A, Gray A, Tam AW, Yang·Feng T, Tsubokawa M, Collins C, Henzel W, Le Bon T, Kathuria S, Chen E. Insulin-like growth factor I receptor primary structure: comparison with insulin receptor suggests structural determinants that define functional specificity. EMBO J 1986; 5: 2503- 2512.
- Abbott AM, Bueno R, Pedrini MT, Murray JM, Smith RJ. Insulin·like growth factor I receptor gene structure. J Bioi Chem 1992; 267: 10759-10763.
- Of Ercole AJ. Insulln·like growth factors and their receptors in growth. Endocrinology & Metabolism, Clin North Am 1996; 25: 573·590.
- Bondy CA. Clinical uses of Insulin-like growth factor-I. Ann Intern Med 1994; 120: 593-601.
- Rechler MM. The nature and regulation of the receptors for insulin-like growth factors. Ann Rev Physiol 1985; 47: 425-442.
- Hintz RL. Role of growth hormone and insulin-like growth factor binding proteins. Horm Res 1990; 33: 105·110.
- Nissley P, Lopczynski W. The insulin-like growth factor receptors. Growth factors 1991; 5: 29·43.
- Blum WF. Insulin-like growth factors and IGF-blndlng proteins: their use for diagnosis of growth hormone deficiency. in: Growth hormone In adults, Juul A, Jorgensen JOL (ads), Cambridge University Press, UK, 1996, pp 48-74.
- Lowe WL. Insulin-like growth factors. Science & Medicine 1996; 3: 62-71.
- Young SC, Miles MV, Clemmons DR. Determinations of the pharmoklnetic profiles of insulin-like growth factor binding protelns-1 and -2 in rats. Endocrinology 1992; 131: 1867-1873.
- Gibson JM, Westwood , Crosby SR, Gordon C, Holly JMP, Fraser W, Anderson C, Young RJ, White A. Choice of treatment affects plasma levels of insulin-like growth factor binding proteln-1 In non-insulin dependent diabetes mellitus (NIDDM). J Clln Endocrinol Metab t995; 80: t369-1375.
- Lee PDK, Jensen MD, Divertie GD, Heiling VJ, Katz HH, Conover CA. Insulin-like growth factor bindIng proteln-1 response to Insulin during suppression of endogenous insulin secret/on.
Metabolism 1993; 42: 409·414.
49, Jones JI, 0' Ercole AJ, Camacho·Hubner C, Clemmons DR. Phosphorylation of insulin-like growth factor bindIng protein In cell culture and In vivo: effects on affinity for IGF-1. Proc Nat/ Acad Sci USA 1991; 88: 7481-7485.
- Clemmons DR. The role of Insulin-like growth factor binding proteins In controlling the expression of IGF actions, In: LeRoith 0, Ralzeda MK (editors), Molecular and Cellular Biology of Insulin-like Growth Factors and their Receptors, Plenum Press, New York, USA, 1989, pp 381-394. 51. Jones JL, Gockerman A, Busby WH, Wright G, Clemmons DR. Insulin-like growth factor binding protein 1 stimulates cell migration and binds to a5fll Integrin by means of its Arg·Gly-Asp
sequence. Proc Natl Acad Sci USA 1993; 90: 10553-10557.
- Rechler MM. Non-receptor-blndlng proteins for Insulin-like growth factors and other cytokines: modulators of peptide action. In: Weintraub BO (editor), Molecular Endocrinology, basic concepts and clinical correlations, Raven Press, New York, USA, 1995, pp 155-180. 53. Rechler MM. Insulin-like growth factor binding proteins. Vitamins and Hormones, 1993; 47: 1-114.
- Baxter RC, Martin JL. Structure of the Mr 140,000 growth-hormone·dependent Insulin-like growth factor binding protein complex: determination by reconstitution and affinity labeling. Proc Natl Acad Sci USA 1989; 86: 6898·6902.
- Guier HP, Zapf J, Schmid C, Froesch ER. Insulin-like growth factors I and II In healthy man. Estimations of half·lives and production rates. Acta Endocrinol (Copenh) 1989; 121: 753-758.
- Buckbinder L, Talbott R, Velasco-Miguel S, Takenaka I, Paba B, Seizinger BR, Kley N. Induction of the growth inhibitor IGF-binding protein 3 by p53, Nature 1995; 377: 646-649.
- Clemmons D. Age-related changes in lOP-I levels, p854-855. In: LeRoith D, moderator, Insulinlike growth factors in health and disease. Ann Intern Med 1992; 116: 854-862.
- IuuI A. Serum levels of IGF-I and IGFBP-3 in healthy children, adolescents and adults. Methodological aspects and definition of reference values with special emphasis on puberty. Ph D Thesis, University of Copenhagen, 1995.
- Hall K, Johansson BL, Povoa G, Thalme B. Serum levels of insulin-like growth factor (lOF) I, H. and IGF binding protein in diabetic adolescents treated with continuous subcutaneous insulin infusion. I Intern Med 1989; 225: 273*278.
- Winter RJ, Phillips LS, Klein MN, Traisman HS, Green ~C. Somatomedin activity and diabetic control in children with insulin-dependent diabetes mellitus. Diabetes 1985; 34: 156-160.
- Lanes R, Recker B. Fort P, Lifshitz F. Impaired somatomedin generation test in children with Insulln·dependent diabetes mellitus. Diabetes 1985; 34: 810-815.
- Dccr Research Group. The effect of Intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Eng! J Med 1993; 329: 977-986.
63. Weiss 0, Anner H, Nephesh I, Alayoff A, Bursztyn M, Raz I. Insulln·like growth factor-I (IGF-I) and IGF-I receptor gene expression In the kidney of the chronIcally hypoinsulinemlc rat and hyperinsullnemlc rat. Metabolism 1995; 44: 982-986
**********************************************************************************************************
IGFs – Insulin Growth Factors
The insulin-like growth factors (IGFs) were discovered in 1956 by William D. Salmon Jr. and William H. Daughaday at Washington University, St Louis, USA (1).
Initially IGFs were called sulfation factors because they were able to replace the sulfation factor activity of growth hormone (GH)(l).
Moreover, the IGFs were found to be able to stimulate DNA synthesis (2), proteoglycan synthesis (3), glycosaminoglycan synthesis (4), and protein synthesis (5).
In 1963 Froesch et al. from the University of ZOrich, Switzerland, described excess insulin-like activity in serum (6). Only a small fraction of the insulin-like activity by normal serum on adipose tissue and muscle could be blocked by specific antibodies against insulin. The mediator of this excess insulin-like activity was not detectable with the radioimmunoassay developed for insulin in 1959 and was termed non-suppressible insulin-like activity (NSILA)(6).
Dulak and Temin demonstrated that serum-free medium conditioned by a rat hepatoma cell line contained mitogenic activity, which they termed multiplication stimulating activity (MSA) (7).
In 1972 these three apparently distinct peptides (sulfation factor, NSILA, MSA) were unified under the term somatomedin, because it apparently mediated the actions of GH (also called somatotropin) (8).
In 1978 Rinderknecht and Humbel purified somatomedin from serum, and it turned out to be two closely related peptides, which were termed Insulin-like growth factor-I (IGF-I) and Insulin-like growth factor-II (IGF-II) (9, 10).
Evolutionary aspects
The IGF-I molecule is highly conserved throughout vertebrate evolution (11).
Amphioxus, a protochordate, expresses a hybrid insulin/IGF-I molecule (12). This strongly suggests that IGF-I diverged from the main line of insulin evolution at a stage antedating the jawless vertebrates.
IGF-I gene stucture and expression
In humans the IGF-I gene is a single gene copy located on chromosome 12 and consists of at least six exons (13). Although the liver was traditionally considered to be the sole producer of IGF-I, recent studies have shown that most tissues express IGF-I (14). Expression of IGF-I mRNA resulting from different transcription initiation sites is tissue-specific, and developmentally and hormonally regulated (11).
Stuctural aspects of IGF-I
IGF-I, IGF-II and insulin are members of a family of polypeptides which are characterized by a high degree of sequence homology (15) (see figure 1). IGF-I is 50·60 % homologous with human pro insulin (16). IGF-I is synthesized as a larger prepro-IGF-I molecule containing a signal peptide as well as a carboxy-terminal extension peptide, the E peptide (17). The signal and E peptide are cleaved off during processing of the mature IGF-I (17). Mature IGF-I is a 70 amino acid peptide, which is different from insulin; at the carboxy terminus it contains an
additional sequence the D domain (18).
Predicted structure of the insulin-like growth factor family of peptides. The heavy line represents the A chain, double lines represent a D extension to the A chain or the C chain joining the A and B chains (from: LeRoith D. Insulinlike growth factors in health and disease. Ann Intern Med 1992; 116: 855; with permission from the American College of Physicians)
IGF-I purified from brain, bovine colostrum, and uterus lacks three aminoterminal amino acid residues (gly-pro·glu) (19). This truncated form of IGF-I, called des-IGF-I, has a much greater biological potency than mature IGF-I because it has a lower affinity for the insulin-like growth factor binding proteins (IGFBPs) (see infra). It is therefore more available for interacting directly with the IGF-I receptor. The cleavage of the tripeptide presumably occurs as a posttranslational event, although the biomechanisms responsible have not yet been identified.
Functions of IGF-I
IGF-I exerts many biological functions on distant target tissues via the blood stream (endocrine effects), on its own cells of origin (autocrine effects), and on neighboring tissues (paracrine effects) (20). IGF-I has both anabolic and mitogenic effects in vitro and in vivo, which often overlap with the biological effects of insulin (Table 1) (20-23): IGF-I stimulates cell differentiation and it is a mitogen for most cultured cells stimulating ['H] thymidine incorporation into DNA and ['H] uridine incorporation into RNA (21). In vitro glucose uptake, amino acid uptake and ion fluxes are increased by IGF-I (21).
In vivo, IGF-I promotes longitudinal bone growth and suppresses GH and insulin secretion (20). IGF-I infusions in normal volunteers increases glucose uptake, reduces free fatty acid and triglyceride levels, and decreases protein breakdown (20). Moreover, insulin stimulates the constitutive secretion of IGF-I from the liver (24). IGF-I in turn, suppresses insulin secretion
even in euglycemic conditions (25). In calorically restricted patients administration of IGF-I improves nitrogen balance (26). IGF-I increases glomerular filtration rate and renal plasma flow and enhances creatinine clearance (27).
IGF-I thus influences many cell functions and is considered as growth factor and hormone with important anabolic and metabolic regulatory functions. Another action of IGF-I which is complementary to its stimulatory effect on cell proliferation, is its capacity to inhibit programmed cell death in certain cells, the so called apoptosis (28, 29).
The free Insulin-like growth factor-I concentration
Free IGF-I, by analogy with sex and adrenal steroids and thyroid hormones, may be a major biological active hormonal form of IGF-I (30) (Figure 2). Determination of serum free unbound IGF-I was not possible until very recently (30, 31). In 1994 Frystyk et a!. and Lee et a!. separately described a method to determine free unbound IGF-I in serum (30, 31).
Distribution of IGFs in serum. Ninety-five percent of the IGFs are found as part of the ternary complex of IGF-I and IGF-II bound to IGFBP-3 and acid-labile subunit (ALS). Less than 5% are bound to other IGFBPs, and a very small component circulates as the free form (from: Collett-Solberg PF, Cohen P.
The role of insulin-like growth factor binding proteins and the IGFBP proteases in modulation of IGF action. Endocrinol Metab Clin North Am 1996; 25: 593; with permission from WB Saunders)
The method of Frystyk et coworkers used ultrafiltration under in vivo conditions (physiological pH, ionic milieu and temperature) to measure IGF-I, while the free IGF-I assay of Lee and coworkers is an IRMA which initially needs no sample extraction as part of the standard procedure to measure IGF-I. Samples are added directly to tubes containing a dense coating of
high-affinity free IGF-I antibody, incubated for 2 hr at room temperature, washed, incubated with a labeled antibody directed to a second epitope, washed and counted. It is likely that the free IGF-I fraction measured with this assay is a combination of the true free and the fraction of IGF-I which can be readily dissociated from IGFBPs under the specific assay conditions (31).
Most circulating IGF-I is bound to the insulin-like growth factor binding proteins (IGFBPs), which titrate the supply of IGF-I to its receptors in the target tissues, while a very small component circulates as the free form (32). The levels of free IGF-I in a system are modulated by the rate of IGF-I production, clearance, and degree of binding to IGFBPs (33). The metabolic clearance of serum free IGF-I is estimated as 2.62 ± 0.94 ml/min with a production rate of 4.75 ± 1.74 mg/day (621 ±227.34 nmol/day) (34). IGF-I bioavailability is probably an important factor in determining the different physiological functions served by IGF-I and insulin (20).
The IGF-I receptor
There are at least two classes of insulin-like growth factor receptors: the insulin· like growth factor-I (IGF-I) receptor and the IGF 11/ mannose -6-phosphate (Man-6-P) receptor (35). The IGF-I receptor gene, like the insulin receptor gene, consists of 22 exons (36). It is the product of a single copy gene located at the distal arm of chromosome 15 (37). The insulin-like growth factor receptors are expressed in many cells and in many tissues (38). The overlapping biological effects of IGFs and insulin were initially attributed to the structural homologies
between the peptides themselves, but this interpretation turned out to be too simple, after it was shown that the receptors for insulin and IGF-I are also structurally similar (39) (Figure 3).
Figure 3
The IGF family of circulating peptides (from: Lowe WL. Insulin-like growth factors. Science & Medicine 1996; 3: 65; with permission from Science & Medicine)
Moreover, IGF-I, IGF-II and insulin can crossreact with each other's receptors (Figure 3) (15). The IGF-I receptor preferentially binds IGF-I, but also binds IGF-II and more weakly insulin. The IGF-II receptor binds IGF-II with higher affinity than IGF-I, but does not interact with even high concentrations of insulin (40). Because IGF-I, IGF-II and insulin can produce the same biological responses, and because many cells possess IGF-I, IGF-II as well as insulin receptors, it has been difficult to determine which receptor is mediating a particular response (40).
Attempts to assess the relative contributions of these three receptors to an observed biologic response have included 1] determination of the receptors present on a cell type and the binding affinities for these three ligands, 2] determination of the biological dose response to IGF-I, IGF-II and Insulin and 3] selective blockade of IGF-I or insulin receptors with specific antireceptor antibodies without intrinsic biological effects (40). These investigations have yielded the insight that insulin and the IGFs are complementary hormones in their anabolic action: insulin and the insulin receptors are especially involved in the regulation of the
short term fluctuations of major metabolites such as glucose, amino acids and free fatty acids. The IGFs and the IGF-I receptor are especially involved in the regulation of the long term processes which are responsible for cell growth and differentiation (41).
In some tissues and cells expressing high numbers of both IGF-I and insulin receptors, hybrids may form (11). These hybrids are tetrameric receptors consisting of an a-f3 heterodimer of the insulin receptor linked by disulfide bonds to a-f3 heterodimer of the IGF-I receptor. A possible role for these hybrid receptors is that they might mediate overlapping functions in which insulin, under certain circumstances, may induce cellular proliferation and IGF-I may stimulate metabolic
functions (11).
It is assumed that most of the biological effects of IGF-II are mediated through the IGF-I receptor (42). However, IGF-I-mediated intracellular signaling has at present only been demonstrated for the IGF-I receptor (also called the type 1 IGF-I receptor) (20).
The insulin-like growth factor binding proteins (IGFBPs).
The IGFBPs are a family of proteins that non-covalently bind IGF-I and IGF-Ii with high affinity (dissociation constants in the order of magnitude 10-11 moilL) and specificity (Table 2) (43, 44). To date at least six IGFBPS have been identified (20, 33). They have a high degree of sequence homology (44) and are numbered 1 to 6 in the order in which their primary structure was determined (45)(Figure 3).
The IGFBPs have been proposed to have four major functions that are essential to coordinate and regulate the biological activities of the IGF-I: lJ to act as transport proteins in plasma and to control the efflux of IGF-I and IGF-Ii from the vascular
space; 2J to prolong the half-life of IGF-I and IGF-Ii and thereby regulating its metabolic clearance; 3J to provide a means of tissue- and cell-type specific localization; 4J to directly modulate interaction between IGF-I and the IGF-I receptor, thereby indirectly controlling its biological actions (20). IGFBPs not only regulate the bioavailability of IGF-I but also seem to have their own receptors, which mediate IGF-I- independent actions (33). IGFBPs are produced by a variety of different tissues, each of which contain specific levels of these IGFBPs (33).
The cleavage of IGFBPs by IGFBP-protease plays a key role in modulating free IGF-I and IGFBP levels and actions by two mechanisms: lJ IGFBP binding to IGFs decrease the concentration of free IGF-I available to interact with the IGF-I receptor, 2J cleavage of the IGFBPs into fragments with lower affinity to IGF-I allows for increased receptor activation (33). In various biological systems the IGFBPs have been shown to inhibit or potentiate IGF-I action (41).
IGFBP-l and IGFBP-3 are discussed more extensively, because the role of the four other binding proteins is less well established at present. IGFBP-l is a 25 Kd protein and found in high concentrations in amniotic fluid (32). IGFBP-l is secreted by hepatocytes, kidney, decidua and endometrium (33). The half-life in plasma is approximately 90 minutes (46). IGFBP-l has been proposed as an acute regulator of IGF-I activity (47). Insulin is a major regulator of hepatic IGFBP-l production (33): plasma IGFBP-l levels are inversely related to insulin levels in vivo (48).
IGFBP-l exists in different forms (phosphorylated and non-phosphorylated) (49). Non-phosphorylated IGFBP-l has a 4- to 6-fold lower affinity to IGF-I than phosphorylated IGFBP-l (49). This would favor sequestration of IGF-I by phosphorylated IGFBP-l and a more complete release of IGF-I to the IGF-I receptor by the non-phosphorylated form. Most studies have shown inhibition of IGF-I activity by IGFP-l (20). The IGFBP-l form which potentiates IGF-I activity is non-phosphorylated, has a lower affinity and is able to associate with the cell surface (50). IGFBP-l stimulates cell migration by itself (51). The stimulus appears to be the binding of IGFBP-l to an integrin on the cell surface, initiating an intracellular pathway which involves a series of kinases (45).
Quantitatively the most important IGFBP in the circulation is IGFBP-3 (52). The 150 kD complex consists of IGF-I (or IGF-II) , IGFBP-3, and an acid-labile subunit (ALS) that is glycosylated and does not bind IGF-I (53). The ALS is present in excess in human plasma and is growth hormone dependent (53, 54). IGFBP-3 is secreted by hepatocytes and many other cells. About 75-95 % of IGF-I in the circulation is carried in the 150 kD IGF-I-IGFBP3- complex (20, 33) (see figure 2). It is considered as a reservoir for IGF-I in the circulation: The 150 kD complex cannot cross the endothelial barrier of the blood vessels (52). This is considered critical for avoiding potential hypoglycemic insulin-like effects of the high concentrations of IGF-I which are present in plasma (52)_ The binding of IGF-I within the the 150 kD complex extends its half life time in the plasma from 10 minutes in the free form to 12 to 15 hours if bound in the complex form (55).
The expression of the gene for IGFBP-3 is Increased by p53, the well characterized product of a tumor suppressor gene, which is considered important in the inhibition of tumor formation (56). Recently it has been demonstrated that p53 increases IGFBP-3 production by cells and that the IGFBP-3 produced in response to p53 is able to inhibit IGF-I induced growth of cells (56). IGFBP-3 thus appears one of those proteins which mediate the effects of p53 on cell growth, possibly by apoptosis.

Figure 4
The relations between IGF·I, IGFBPs, growth hormone and insulin{from: Bondy CA. Clinical uses of insulin-like growth factor-I. Ann Intern Med 1994; 120: 594; with permission from the American College of Physicians)
Growth hormone (GH) and insulin both stimulate hepatic IGF-I production, and IGF-I feeds back to suppress GH and insulin release. IGFBP-3 and the associated acid-labile subunit (ALS) are positively regulated by GH, whereas IGFBP-1 levels are negatively regulated by insulin (40) (Figure 4).
IGF-I and age
Age is a major determinant of plasma IGF-I concentrations (57). Serum levels of IGF-I increase significantly from very low levels in cord serum through the first 9 months of life, whereafter there is an almost linear increase from early Serum IGF·I levels (vertical axis) according to age (horizontal axis) throughout life in a healthy population (n=1236 subjects).
Note the peak at puberty and the wide range of IGF·I levels at each age (from Juul A. Serum levels of IGF·I and IGFBp·3 in healthy children, adolescents and adults. Methodological
aspects and definition of reference values with special emphasis on puberty (Ph D Thesis, University of Copenhagen, 1995; with permission of NovoNordisk, Denmark) childhood into adolescence (Figure 5) (58). After puberty, a 2.5·fold decrease occurs in the mean IGF·I values by the third decade, and a further twofold decrease occurs between the third and eights decade (57). Part of this decrement is believed to be due to the known age·related decrease in GH secretion (57). Very little is known on the effects and clinical consequences of the decrease of the GH· IGF·I system during aging.
IGF-I and diabetes
Many patients with insulin-dependent diabetes mellitus type 1 have some degree of growth hormone resistance, as shown by lowered circulating IGF-I levels, despite increased GH concentrations (59-61). They lack the ability to produce an appropriate increase in IGF-I response to exogenous GH. This functional refractoriness to GH is also seen during starvation and may be due to lowered portal vein insulin concentrations, insufficient to stimulate normal hepatic IGF-I synthesis (40). Treatment with subcutaneous insulin injections may not normalize
all liver functions, such as IGF-I synthesis, which mainly depends on the presence of high portal insulin levels (40). In addition, increased growth hormone levels exacerbate hyperglycemia and low IGF-I levels may also contribute to deficient glucose metabolism and hyperglycemia (40).
Hyperglycemia is considered as an important pathogenetic factor for the development of diabetic micro- and macrovascular complications (62). The DCCTtrial has suggested that treatment of type I diabetic patients that does not result in normoglycemia will not prevent the development and progression of diabetic complications. Moreover, it has been reported in an animal model of diabetes that glucose levels playa major role in the regulation of IGF-I receptor mRNA (63)_ After hyperglycemia an increase in IGF-I receptor mRNA was observed, which was reversible by normoglycemia, even after long-standing hyperglycemia.
References
1. Salmon WO, Oaughaday WHo A hormonally controlled serum factor which stimulates sulfate incorporation by cartilage in vitro. J Lab Clin Med 1957; 49: 825-836.
2. Oaughaday WH, Reeder C. Synchronous activation of DNA synthesis In hypophysectomized rat cartilage by growth hormone. J Lab Clin Med 1966; 68: 357-368.
3. Hall K, Uthne K. Some biological properties of purified sulfation factor (SF) from human plasma.
Acta Med Scand 1971; 190: 137-143.
4. Oaughaday WH, Philips LS, Herington AC. Measurement of somatomedln by cartilage in vitro.
Methods Enzymol 1975; 37B: 93·109.
5. Salmon jr WO, Duvall MR. In vitro stimulation of leucine incorporation into muscle and cartilage protein by a serum fraction with sulfation factor activity: differentiation of effects from those of growth factor and Insulin. Endocrinology 1970; 87: 1168-1180.
6. Froesch ER, BOrgi H, Ramseier EP, Bally P, labhart A. Antibody suppressible and insulin-like activities In human serum and their physiological significance. An insulin assay with adipose tissue of increased precision and specificity. J Clin Invest 1963; 42: 1816-1834.
7. Dulak NC, Temin HM. A partially purified polypeptide fraction from rat liver cell conditioned medium with multiplication·stimulating activity for embryo fibroblasts. J Cell Physiol1973; 81: 153- 160.
8. Daughaday WH, Hall K, Raben MS, Salmon WD, van den Brande JL, van Wyk JJ. Somatomedin: proposed designation for sulfation factor. Nature 1972; 235: 107-108.
9. Rinderknecht E, Humbel RE. The amino acid sequence of human Insulin-like growth factor I and its structural homology with proinsulin. J Bioi Chem 1978; 253: 2769-2776.
10. Rinderknecht E, Humbel RE. The primary structure of hUman insulin-like growth factor II. FEBS Letters 1978; 89: 283-286.
11. LeRoith D, Adamo M, Werner H, Roberts CT. Molecular and cellular biology of the Insulin·like growth factors, in: Weintraub BO (editor), Molecular Endocrinology, basic concepts and clinical correlations, Raven Press, New York, USA, 1995, pp 181-193. 12. Chan SJ, Cao Q-P, Steiner OF. Evolution of the insulin superfamily: cloning of a hybrid Insulin/lnsulin-like growth factor cDNA from amphioxus. Proc Natl Acad Sci USA 1990; 87: 9319-
9323.
13. Brissenden JE, Ulrich A, Francke U. Human chromosomal mappIng of genes for insulin-like growth factors I and 11 and epidermal growth factor. Nature 1984; 310: 781-784.
14. LeRoith O. Insulin-like growth factors in health and disease. Ann Intern Med 1992; 116: 854- 862.
15. Froesch 'ER, Zapf J. Insulin-like growth factors and insulin: comparative aspects. Diabetologla 1985; 28: 485·493.
16. Van den Brande Jl. Structure of the human Insulin-like growth factors: relationship to function. In: Schofield PN (editor), The insulin-like growth factors, structure and biological functions, Oxford University Press, Oxford, UK, 1992, pp 12-44.
17. Daughaday WH, Rotwein P. Insulin-like growth factors I and II. Peptide, messenger ribonucleic acid and gene structures, serum, and tissue concentrations. Endocr Rev 1989; 10: 68-91.
18. Sara VR, Hall K. Insulin·like growth factors and their binding proteins. Physiol Rev 1990; 70: 591-594.
19. Sara VR, Carlsson-Skwirut C, Andersson C, Hall E, Sjogreb B, Holmgren H, Jornvall H. Characterization of somatomedlns from human fetal brain; Identification of a variant form of insulinlike growth factor I. Proc Nail Acad Sci USA; 1986; 83; 4904-4907.
20. Jones JI, Clemmons DR. Insulin-like growth factors and their binding proteins: biological actions. Endocr Rev 1995; 16:3-34. 21. Kless W, Kessler U, Schmitt S, Funk B. Growth hormone and Insulin-like growth factor-I: Basic aspects. In: Flyvbjerg A, 0rskov H, Alberti KGGM (editors), Growth hormone and inSUlin-like growth factor-' in human and experimental diabetes, John Wiley & Sons, Chlcester, UK, 1993, pp 1-21.
22. Froesch ERr Schmid C, Schwander J, Zapf J. Actions of insulin-like growth factors. Ann Rev Physiol1985; 47: 443·467.
23. Kahn CR. The molecular mechanism of Insulin action. Ann Rev Med 1965; 36: 429·451.
24. Phillips LS, Harp JBr Goldstein S, Klein J, Pao CI. Regulation and action of Insulin·like growth factors at the cellular level. Proc Nutr Soc 1990; 49: 451-456.
25. Rennert NJ, Caprio S, Sherwin RS. Insulin·like growth factor-I inhibits glucose-stimulated insulin secretion but does not impair glucose metabolism in normal humans. J Clin Endocrinol Metab 1993; 76: 804·806.
26. Clemmons DR, Smith· Banks A, Underwood LE. Reversal of diet-induced catabolism by infusion of recombinant insulin·like growth factor-I (IGF-I) in humans. J Clin Endocrinol Metab 1992; 75: 234- 238.
27. Hirschberg R Brunori G, Kopple JD, Guier HP. Effects of insulin-like growth factor I on renalfuncUon In normal men. Kidney Int 1993; 43: 367-397,
28. Muta K, Krantz SB. Apoptosis of human erythroid colony forming cells is decreased by stem cell factor and insulin· like growth factor-I as well as erythropoietin. J Cell Physlol 1993; 156: 264-271.
29. Kaleko M, Rutter WJ, Miller AD. Overexpresslon of the insulinlike growth factor receptor promotes ligand-dependent neoplastic transformation. Mol Cell Bioi 1990; 10: 464·473.
30. Frystyk J, Skjrerbrek C, Dlnesen B, 0rskov H. Free Insulin·like grow1h factors (IGF-I and IGF·II) in human serum. FEBS letter 1994; 348,185-191. 31. Lee PDK, Powell 0, Baker B, Liu F, Mathew G, Levitsky I, Gutierrez 00, Hintz RL.
Characterization of a direct, non·extractlon Immunoradiometric assay for free IGF-1. Abstract 939, Presented at the 76th annual meeting of the Endocrine Society, Anaheim 1994.
32. Drop SL, Kortleve OJ, Guyda HJ. Isolation of a somatomedin·blnding protein from preterm amniotic fluid. Development of a radioimmunoassay. J Clin Endocrinol Metab 1984; 59: 899-907.
33. Collett-Solberg PF, Cohen P. The role of insulin·like growth factor binding proteins and the IGFBP proteases in modulation of IGF action. Endocrinol Metab CUn North Am 1996; 25: 591-614.
34. Boroujerdl MAt Jones RH, Sonksen PH, Russell·Jones DL. Stimulation of IGF·I pharmacokinetics after infusion of recombinant IGF-Iln human subjects. Am J Physiol 1997; 273: E438·E447.
35. Baxter RC. Insulin-like growth factor binding proteins in human circulation, a review. Horm Res 1994; 42: 140-144.
36. Undenwood LE, van Wyk JJ. Normal and aberrant grow1h. In: Wilson JD, Foster OW (editors), Williams Textbook of Endocrinology, WB Saunders Company, Philadelphia, USA, 1992, pp 1079· 1138.
37. Ullrich A, Gray A, Tam AW, Yang·Feng T, Tsubokawa M, Collins C, Henzel W, Le Bon T, Kathuria S, Chen E. Insulin-like growth factor I receptor primary structure: comparison with insulin receptor suggests structural determinants that define functional specificity. EMBO J 1986; 5: 2503- 2512.
38. Abbott AM, Bueno R, Pedrini MT, Murray JM, Smith RJ. Insulin·like growth factor I receptor gene structure. J Bioi Chem 1992; 267: 10759-10763.
39. Of Ercole AJ. Insulln·like growth factors and their receptors in growth. Endocrinology & Metabolism, Clin North Am 1996; 25: 573·590.
40. Bondy CA. Clinical uses of Insulin-like growth factor-I. Ann Intern Med 1994; 120: 593-601.
41. Rechler MM. The nature and regulation of the receptors for insulin-like growth factors. Ann Rev Physiol 1985; 47: 425-442.
42. Hintz RL. Role of growth hormone and insulin-like growth factor binding proteins. Horm Res 1990; 33: 105·110.
43. Nissley P, Lopczynski W. The insulin-like growth factor receptors. Growth factors 1991; 5: 29·43.
44. Blum WF. Insulin-like growth factors and IGF-blndlng proteins: their use for diagnosis of growth hormone deficiency. in: Growth hormone In adults, Juul A, Jorgensen JOL (ads), Cambridge University Press, UK, 1996, pp 48-74.
45. Lowe WL. Insulin-like growth factors. Science & Medicine 1996; 3: 62-71.
46. Young SC, Miles MV, Clemmons DR. Determinations of the pharmoklnetic profiles of insulin-like growth factor binding protelns-1 and -2 in rats. Endocrinology 1992; 131: 1867-1873.
47. Gibson JM, Westwood , Crosby SR, Gordon C, Holly JMP, Fraser W, Anderson C, Young RJ, White A. Choice of treatment affects plasma levels of insulin-like growth factor binding proteln-1 In non-insulin dependent diabetes mellitus (NIDDM). J Clln Endocrinol Metab t995; 80: t369-1375.
48. Lee PDK, Jensen MD, Divertie GD, Heiling VJ, Katz HH, Conover CA. Insulin-like growth factor bindIng proteln-1 response to Insulin during suppression of endogenous insulin secret/on.
Metabolism 1993; 42: 409·414.
49, Jones JI, 0' Ercole AJ, Camacho·Hubner C, Clemmons DR. Phosphorylation of insulin-like growth factor bindIng protein In cell culture and In vivo: effects on affinity for IGF-1. Proc Nat/ Acad Sci USA 1991; 88: 7481-7485.
50. Clemmons DR. The role of Insulin-like growth factor binding proteins In controlling the expression of IGF actions, In: LeRoith 0, Ralzeda MK (editors), Molecular and Cellular Biology of Insulin-like Growth Factors and their Receptors, Plenum Press, New York, USA, 1989, pp 381-394. 51. Jones JL, Gockerman A, Busby WH, Wright G, Clemmons DR. Insulin-like growth factor binding protein 1 stimulates cell migration and binds to a5fll Integrin by means of its Arg·Gly-Asp
sequence. Proc Natl Acad Sci USA 1993; 90: 10553-10557.
52. Rechler MM. Non-receptor-blndlng proteins for Insulin-like growth factors and other cytokines: modulators of peptide action. In: Weintraub BO (editor), Molecular Endocrinology, basic concepts and clinical correlations, Raven Press, New York, USA, 1995, pp 155-180. 53. Rechler MM. Insulin-like growth factor binding proteins. Vitamins and Hormones, 1993; 47: 1-114.
54. Baxter RC, Martin JL. Structure of the Mr 140,000 growth-hormone·dependent Insulin-like growth factor binding protein complex: determination by reconstitution and affinity labeling. Proc Natl Acad Sci USA 1989; 86: 6898·6902.
55. Guier HP, Zapf J, Schmid C, Froesch ER. Insulin-like growth factors I and II In healthy man. Estimations of half·lives and production rates. Acta Endocrinol (Copenh) 1989; 121: 753-758.
56. Buckbinder L, Talbott R, Velasco-Miguel S, Takenaka I, Paba B, Seizinger BR, Kley N. Induction of the growth inhibitor IGF-binding protein 3 by p53, Nature 1995; 377: 646-649.
57. Clemmons D. Age-related changes in lOP-I levels, p854-855. In: LeRoith D, moderator, Insulinlike growth factors in health and disease. Ann Intern Med 1992; 116: 854-862.
58. IuuI A. Serum levels of IGF-I and IGFBP-3 in healthy children, adolescents and adults. Methodological aspects and definition of reference values with special emphasis on puberty. Ph D Thesis, University of Copenhagen, 1995.
59. Hall K, Johansson BL, Povoa G, Thalme B. Serum levels of insulin-like growth factor (lOF) I, H. and IGF binding protein in diabetic adolescents treated with continuous subcutaneous insulin infusion. I Intern Med 1989; 225: 273*278.
60. Winter RJ, Phillips LS, Klein MN, Traisman HS, Green ~C. Somatomedin activity and diabetic control in children with insulin-dependent diabetes mellitus. Diabetes 1985; 34: 156-160.
61. Lanes R, Recker B. Fort P, Lifshitz F. Impaired somatomedin generation test in children with Insulln·dependent diabetes mellitus. Diabetes 1985; 34: 810-815.
62. Dccr Research Group. The effect of Intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Eng! J Med 1993; 329: 977-986.
63. Weiss 0, Anner H, Nephesh I, Alayoff A, Bursztyn M, Raz I. Insulln·like growth factor-I (IGF-I) and IGF-I receptor gene expression In the kidney of the chronIcally hypoinsulinemlc rat and hyperinsullnemlc rat. Metabolism 1995; 44: 982-986.